治疗脑部疾病时,血脑屏障是一道难以逾越的难关。但西奈山伊坎医学院的研究人员成功研发出一种能够突破这一障碍的偶联物。这一重大突破让人感到非常振奋。这种偶联物有潜力根本性地改变治疗多种神经和精神疾病的方法。
西奈山医学院的创新成果
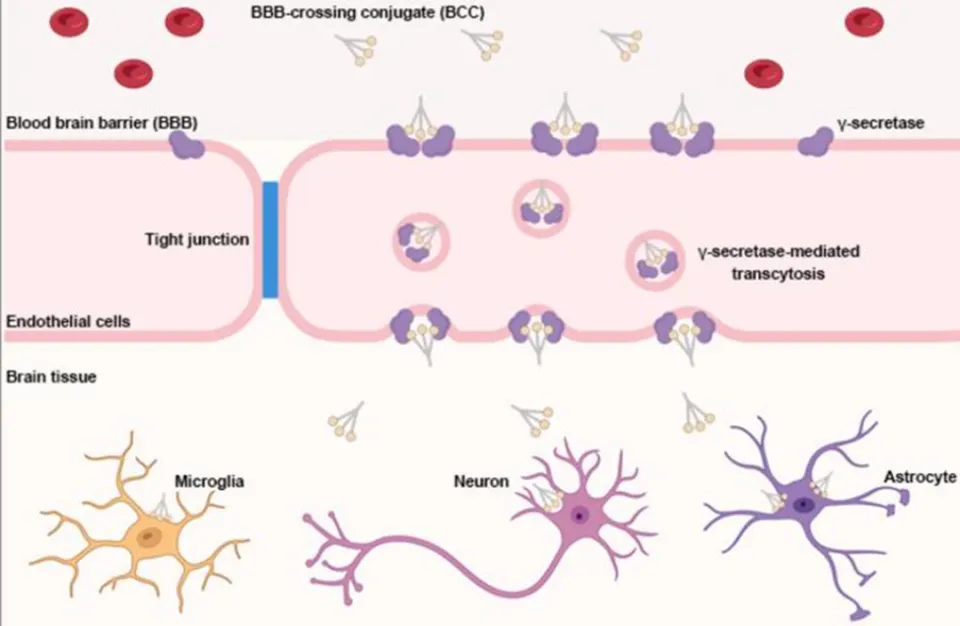
西奈山伊坎医学院研发的这种新型BCC,是一种具有创新性的血脑屏障穿越偶联物。这一成果已发表在《自然》杂志的子刊上。这一发现体现了科学家们在科研道路上的不懈追求和创新精神。这种BCC平台通过特定机制发挥作用,并且能够通过静脉注射将大分子治疗药物直接送达大脑。这在以往是不可能的,该平台的出现标志着科研领域的重大突破。

血脑屏障的作用与阻碍
血脑屏障原本是一道自然的防线,它能有效阻挡有害物质进入大脑。然而,这一功能也使得不少救命药物难以抵达大脑。比如,肌萎缩性侧索硬化症和阿尔茨海默病这类中枢神经系统疾病,治疗时常常遇到血脑屏障的阻碍。这导致全球众多患者难以获得有效治疗,也让无数家庭承受着痛苦和无奈。
BCC的具体治疗实验示例
在BCC治疗实验中,研究人员取得重大进展。他们把BCC10这种化合物与反义寡核苷酸配对,注入小鼠体内后,有效抑制了小鼠大脑中不良基因的活动。在针对ALS的特定转基因小鼠模型上,这种治疗方法明显减少了致病基因Sod1及其相关蛋白的表达。还有,另一种与BCC10结合的反义寡核苷酸也明显降低了阿尔茨海默病关键基因Mapt的表达。这些成果充分展示了BCC在治疗领域的显著效果。
BCC的优异递送效果
BCC10在将大分子药物送至大脑方面效率极高。无论是通过模型实验,还是人体脑组织样本,其递送效果都十分显著。与之前尝试的其他方法相比,BCC10这一特性为大分子药物进入大脑开辟了一条高效的新途径,同时也为脑部疾病的治疗带来了新的希望。
疗法的耐受性良好
研究显示,该疗法在小鼠体内显示出良好的耐受性。在实验所采用的剂量范围内,小鼠的主要器官损伤极为轻微。这表明,若用于人类,引发不良反应的可能性也会相对较小。尽管还需进一步研究以证实,但这一发现已是一个积极信号,预示着该疗法在临床应用上的广阔前景。
后续研究方向
研究团队计划在大动物模型上进行更深入的探索。这一步骤至关重要,因为只有通过大动物模型的研究,该平台才有望应用于临床治疗。这一策略既合理又非常必要。若该平台在大动物模型的研究上取得成功,脑部疾病的治疗可能迎来新的突破,为全球脑部疾病患者带来新的希望。
我想问一下大家,对于这种能突破血脑屏障的先进技术,大家预计它最快能在多少年内应用于临床治疗?期待你们的讨论和看法。另外,别忘了给这篇文章点个赞,还有分享。